Контент только для подписчиков
Открытое овальное окно и дефект межпредсердной перегородки – отверстия в межпредсердной перегородке, которые отличаются по своей морфологией и функциональным последствиям. Соответственно, хотя технические аспекты лечения во многом совпадают, показания – отличаются.
ООО (англ. PFO — potent foramen ovale) состоит из 2 перекрывающихся эмбриологических структур, левосторонней частично фиброзной первичной перегородки и правосторонней мышечной вторичной перегородки, которые формируют овальное отверстие – односторонний щелевой клапан для физиологического сброса справа налево (функционирующий во время внутриутробного периода развития), который расположен внутри овальной ямки. Послеродовое увеличение легочного кровообращения и снижения давления в правом предсердии приводит к немедленному функциональному закрытию овального отверстия путем прилегания первичной перегородки ко вторичной. В течение нескольких месяцев после родов, в большинстве случаев, первичная и вторичная перегородка надежно срастаются в большинстве случаев. Однако, исследования показывают, что овальное отверстие остается открытым примерно у 25% популляции.
В частности, у лиц с аневризмой предсердной перегородки (ASA, врожденная аномалия межпредсердной перегородки, которая характеризуется увеличенной первичной перегородки с ее гипермобильностью и пролабированием в предсерия >10 мм) распространенность ООО увеличивается до 50-85%.
ДМПП (англ. ASD — atrial septal defect) представляет собой второй наиболее распространенный врожденный порок сердца, на который приходится около 10% всех врожденных пороков сердца у взрослого населения. Семейная заболеваемость наблюдается редко, но описана примерно в 2% случаев. Существует связь с генетическими заболеваниями, как синдром Дауна и синдром Холта-Орама.
В зависимости от локализации в предсердной перегородке, ДМПП в основном делятся на четыре разных типа (таблица 1). Вкратце, это:
- ASD Secundum, который является наиболее распространенным типом дефекта предсердной перегородки, расположен в центре или перегородке;
- Primum ASD, второй наиболее распространенный тип, расположен рядом с атриовентрикулярными клапанами и обычно ассоциируется с дефектом клапанов (например, митральной щелью).
- Дефект венозного синуса (Sinus venosus ASD) является дефектом вблизи соединения верхней или нижней кавальной вены и часто связана с аномальной связью правых легочных вен с правым предсердием или верхней полой веной.
- Дефект коронарного синуса — напрямую связывает коронарный синус с левым предсердием.
Все они имеют сходные гемодинамические последствия. Тем не менее, только ASD Secundum можно лечить интервенционно, что и будет обсуждаться в этой статье.
| Тип | Распространенность | Ассоциированные поражения |
| Secundum ASD (ASD II) | 75% | Множественные дефекты |
| Primum ASD (ASD I) | 15% | Дефект атриовентрикулярного клапана |
| Sinus venosus ASD | 10% | Патологический дренаж правых легочных вен |
| Coronary sinus ASD | Редко | Персистирующая левая верхняя полая вена |
Цель данной статьи – предоставить обзор и кратко описать интервенционные техники закрытия открытого овального окна и ДМПП.
[nextpage title=»Показания к интервенционному закрытию»]
Если вкратце, то ООО обычно протекает бессимптомно. Однако его присутствие все чаще признается в качестве своеобразного медиатора для манифестации других заболеваний (Таблица 2). В настоящее время наиболее обоснованным показанием для закрытия ООО является вторичная профилактика инсульта у пациентов без дополнительных потенциальных причин эмболического события (криптогенный инсульт). Несколько исследований показали преимущество интервенционного подхода в данном случае.
Отсутствие значимых различий в исходах, которые были продемонстрированы исследованием CLOSURE I (первое рандомизированное сравнение интервенционной и консервативной тактики лечения пациентов с криптогенным инсультом) могут поставить под сомнение это показание. Однако, из-за существенных недостатков этого исследования, включая использование устаревшего закрывающего устройства, которое, как известно, имеет критический профиль безопасности по сравнению с другими устройствами (STARFlex occluder; NMT Medical Inc., Boston, MA, USA), период наблюдения является слишком коротким для получения значимых результатов в этой ситуации (2 года). Исследования PC и RESPECT с использованием окклюдера Amplatzer доказали эффективность интервенционного подхода, показав снижение частоты инсультов на более чем 75%.
| Открытое овальное окно | Дефект МПП | |
| Общепринятые показания | Парадоксальная эмболия (инсульт/ТИА) | Парадоксальная эмболия (инсульт/ТИА) |
| Декомпрессионная болезнь | Перегрузка правых отделов сердца со значительным шунтом (Qp/Qs > 1.5:1) | |
| Синдром платипноэ-ортодеоксии | ||
| Возможные показания (обсуждаются) | Мигрень с аурой | Маленькие (до 5 мм) или очень большие ( более 35 мм) |
| Синдром обструктивного ночного апноэ | ||
| ТИА – транзиторная ишемическая атака | ||
Результаты продолжающегося исследования REDUCE с окклюдером Helex, исследование DEFENSE-PFO с окклюдером Amplatzer и исследование CLOSE с различными окклюдерами помогут в дальнейшем уточнить обоснованность такого показания.
Мигрень (с аурой) в настоящее время обсуждается как еще одно потенциальное показание к интервенционному закрытию ООО. Открытое овальное окно наблюдается у 50% пациентов с мигренью с аурой. Кроме того, закрытие ООО следует рассматривать у дайверов, у которых риск декомпрессионной болезни в 4,5 раза выше, чем у их дайверов без ООО.
Наличие потенциального шунта справа-налево играет роль в различных патологических состояниях, связанных с гипоксемией – синдроме платипноэ-ортодеоксии или синдроме обструктивного ночного апноэ. В настоящее время ведутся исследования на тему связи связи ООО с мигренью, а также ООО и синдрома обструктивного ночного апноэ. Их результаты, возможно, расширят показания к интервенционному закрытию ООО. Благодаря своей простоте (что будет показано ниже), техника интервенционного закрытия открытого овального окна является методикой выбора в большинстве перечисленных выше сценариев и полностью лишает смысла классическую хирургическую коррекцию ООО.
Первичным обоснованием закрытия ДМПП является устранение гемодинамической правосторонней перегрузки от значительного шунтирования слева направо. Все формы ДМПП обычно характеризуются шунтом слева направо, если только не произошел реверс шунта, наблюдаемое на более поздней стадии; В присутствии значительного шунта (Qp: Qs> 1,5: 1) значительная объемная перегрузка правого предсердия и правого желудочка присутствует даже у педиатрических пациентов, что приводит к растяжению стенок предсердий и правого желудочка и ремоделированию сосудов с неблагоприятными долгосрочными последствиями, такими как предсердные аритмии, миокардиальная недостаточность и легочная гипертензия.
Может наблюдаться спонтанное закрытие ДМПП, поэтому в раннем детстве такие пациенты должны наблюдаться, особенно в случае регрессии размеров и отсутствии неблагоприятных эффектов. У взрослых пациентов закрытие ДМПП значительных размеров показано независимо от возраста. Интервенционное закрытие ДМПП возможно при размере дефекта до 38 мм и отсутствии выраженного «кольца» для хорошей фиксации устройства (более 5мм на протяжении 75% окружности).
Кроме того, чтобы избежать синдромов острой легочной гипертензии и застоя в легких сразу после закрытия устройства, предпроцедурное давление в артериальной артерии должно составлять менее двух третей системного давления, сосудистое сопротивление легких менее двух третей системного сосудистого сопротивления. Также должна присутствовать отзывчивость на вазодилататорную терапию, либо на тестовую окклюзию дефекта. Поэтому закрытие ДМПП у пациентов с шунтом справа налево и тяжелой и фиксированной легочной гипертензией (например, при синдроме Эйзенменгера) противопоказано.
Как и у пациентов с ООО, необходимо подчеркнуть риск парадоксальных эмболов, особенно у взрослых пациентов на фоне повышенного давления в правом предсердии или предсердной аритмии.
[nextpage title=»Методы интервенционного лечения»]
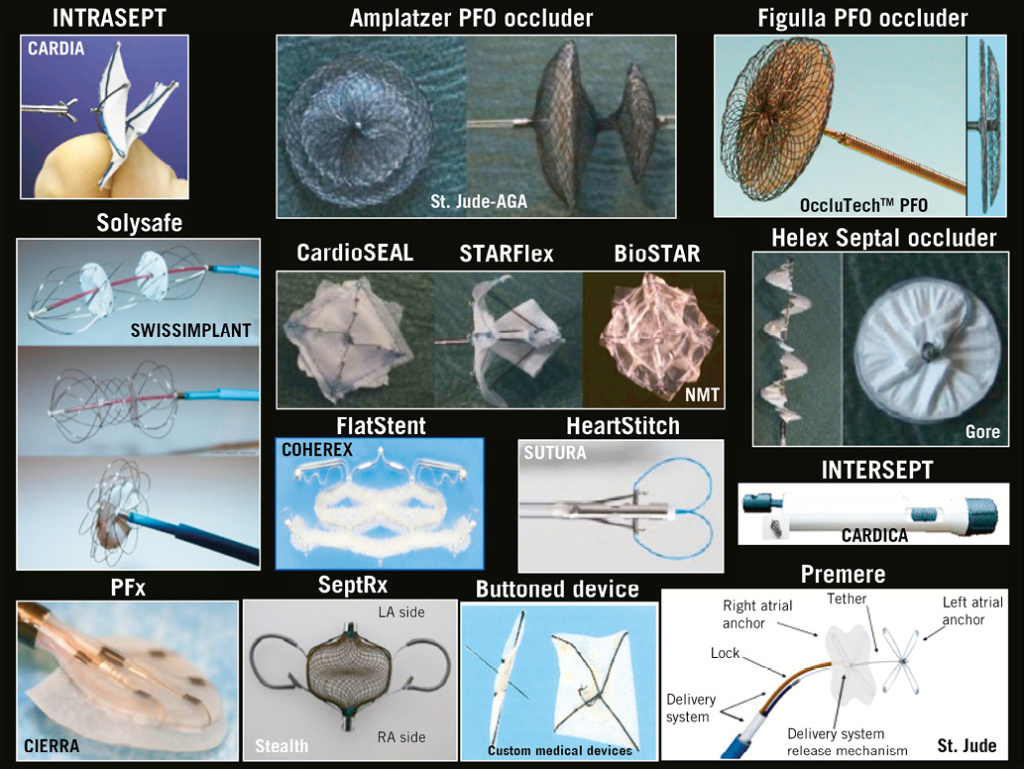
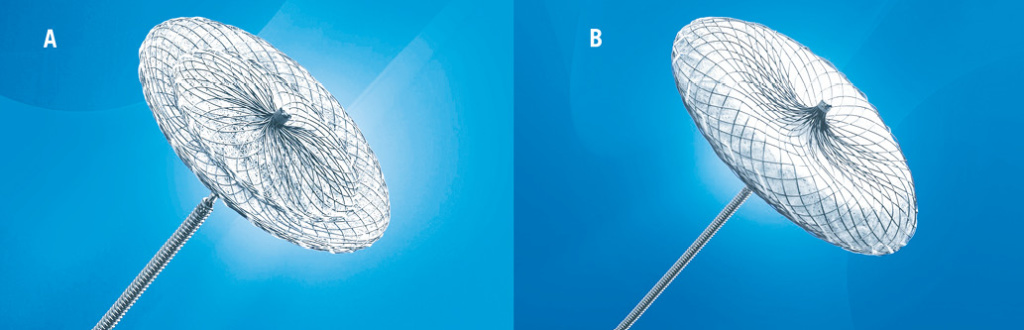
Анатомические и физиологические различия между ООО и ДМПП привели к разработке устройств, предназначенных специально для каждой патологии. Хотя существуют различные альтернативные устройства, особенно на рынке ООО (рисунок 1), наиболее часто используется семейство устройств Amplatzer для закрытия PFO и ASD (рисунок 2). В Соединенных Штатах окклюдер мембраны Amplatzer (ASO) (St. Jude Medical, Plymouth, MN, США) и окклюдер Gore® Helex® (WL Gore & Associates Inc., Flagstaff, AZ, США) одобрены FDA как устройства для закрытия ДМПП. Мы обычно используем устройство ASO, выполненное на основе нитинола, которое доступно в широком диапазоне размеров (от 4 до 40 мм), которое способно извлекаться и развертываться повторно. Благодаря своей «талии» устройство самоцентрируется и обеспечивает полное закрытие почти в 100% случаев. Другие типы устройств направлены на минимизацию металлической поверхности, например, устройства BioSTAR (NMT Medical Inc., Бостон, Массачусетс, США), состоящего из биоразлагаемой ткани или Coherex Flatstent (Coherex Medical, Inc., Salt Lake City, UT, USA ). С этими устройствами следует облегчить будущий доступ к левому предсердию: это важный фактор у пациентов, склонных к фибрилляции предсердий. Однако, несмотря на многоцентровое клиническое исследование с отличными коэффициентами закрытия для BioSTAR, оба устройства не столь универсальны, как устройство ASO. Более того, BioSTAR больше не доступен, поскольку компания вышла из бизнеса.
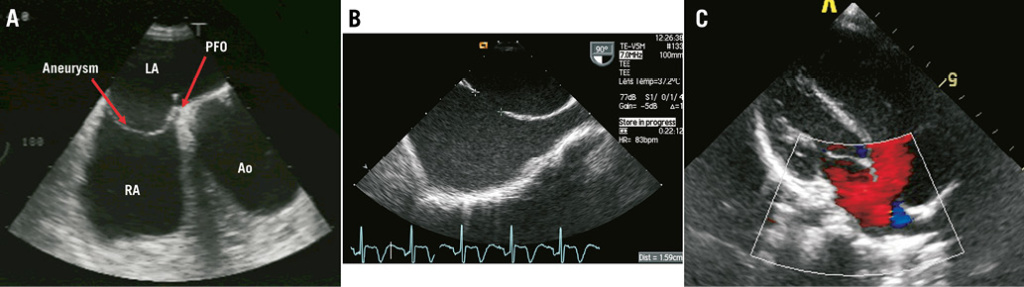
Как правило, перед закрытием дефекта каждый пациент должен пройти ультразвуковое исследование (трансторакально, но желательно — чреспищеводно) для глубокой морфологической оценки с целью уточнения анатомии дефекта. В частности, необходимо уточнить количество, локализацию и размеры дефектов, а также наличие или отсутствие ободка (ободков) вокруг дефекта (дефектов), поскольку это важный фактор для закрепления устройства. Следует подтвердить дренаж легочных вен в левое предсердие и исключить какие-либо другие аномалии.
Процедуру имплантации можно проводить под местной анестезией под контролем флюороскопии, но часто в качестве дополнения используется ультразвуковая визуализация (особенно в случае больших дефектов). Ниже будет подробно описано закрытие ООО и ДМПП с использованием устройства Amplatzer.
[nextpage title=»Техника закрытия открытого овального окна»]
Как правило, ООО легко проходимо под контролем флюороскопии в передне-задней проекции с использованием J-проводника диаметром 0,035 дюйма, или, если требуется, с помощью многоцелевого или аналогичного катетера. Иногда (при небольших размерах ООО) для прохождения дефекта J-образный кончик проводника должен быть выпрямлен (или необходимо использование прямого гидрофильного проводника, но это увеличивает риск перфорации). Проводник помещается в левую верхнюю легочную вену или в левое предсердие. Оценка размера дефекта с помощью баллона (balloon sizing) не рекомендуется, так как максимальное открытие лоскутного (flap-like) ООО не имеет решающего значения для успешного закрытия. Напротив, существует конечный риск разрыва тонкой перегородки во время раздутия баллона.
При использовании окклюдера Amplatzer PFO в большинстве случаев выбирается 25-миллиметровое устройство, за исключением случаев крошечных дефектов с чрезвычайно низкой подвижностью, которые позволяют имплантировать 18-миллиметрового устройства или в случаях очень длинных туннелей и больших дефектов с хрупкими ободками или выраженной вторичной перегородкой, где требуются более крупные окклюдеры. Устройство готовится перед введением интродьюсера, чтобы свести время пребывания последнего в кровотоке к минимальному. Используя окклюдер Amplatzer, устройство сначала завинчивается на кабель толкателя, а затем ослабляется путем отвинчивания на долю поворота для облегчения выпуска устройства позже. Его втягивают в оболочку доставочного интродьюсера (система доставки, loader sheath) под водой, чтобы избежать застревания воздуха. Кончик устройства должен торчать из системы доставки на несколько миллиметров.
Затем систему доставки следует продвигать вместе с расширителем по проводнику до тех пор, пока наконечник оболочки не окажется глубоко в левом предсердии. Чтобы предотвратить всасывание воздуха при удалении расширителя, оболочка для доставки на ее проксимальном конце удерживается ниже уровня сердца, например, поперек бедра пациента. Кроме того, когда удлинитель оболочки отводится назад, проводник удерживается в левом предсердии. Это предотвращает заклинивание торцевого отверстия системы доставки и позволяет крови заполнять просвет катетера, предотвращая непреднамеренное аспирирование воздуха. После удаления расширителя и проводника погрузчик подключается к системе доставки под обратным кровотоком, и устройство продвигается под флюороскопическим контролем (проекция АР) к левому предсердию, продвигая кабель толкателя. Перед тем, как выйти из оболочки, убедитесь, что устройство правильно закручено на кабель толкателя (не слишком плотный и не слишком слабо) и что конец системы доставки свободно располагается в левом предсердии. В отличие от закрытия ДМПП, только левый предсердный диск теперь разворачивается в левом предсердии — либо все еще в проекции AP, которая позволяет видеть положение перегородки с самого начала операции, либо в проекции LAO 60, в которой правый диск будет развернут позже.
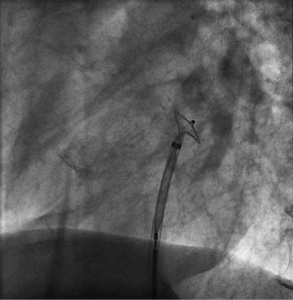
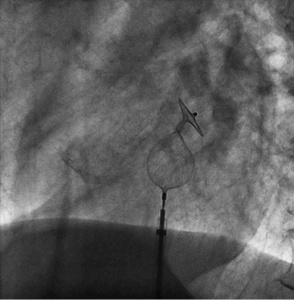
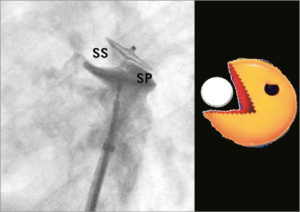
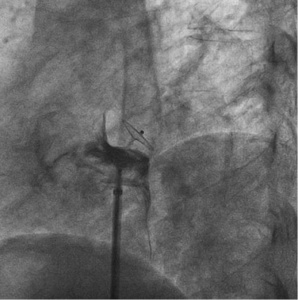
Затем устройство и систему доставки вместе аккуратно оттягивают назад и устанавливают напротив предсердной перегородки — что видно на рентгене за счет изменения угла левого диска, а также ощущается тактильно. Лучше всего использовать проекцию LAO (рисунок 4). Затем правый предсердный диск разворачивается, поддерживая натяжение на толкающем кабеле, одновременно вытягивая систему доставки. Оптимальное позиционирование подтверждается знаком Pacman’а — типичным взаимным расположением развернутых дисков при флюороскопии или эхокардиографией, если они используются (рисунок 6). Для окончательной проверки правильного положения в случаях без использования УЗИ, выполняется контрастирование правого предсердия для четкой визуализации его контуров и положения перегородки, а также уточнения пространственной ориентации устройства (рисунок 7). В эту же съемку рекомендуется визуализировать и левое предсердие. Наконец, устройство проверяется на стабильность небольшим покачиванием, а затем отпускается путем откручивания кабеля толкателя против часовой стрелки. Повторное контрастирование подтверждает окончательный . В опытных руках дополнительная эхокардиографическая визуализация не требуется, особенно если пациент прошел тщательно предпроцедурное ультразвуковое обследование. Однако в случаях сомнительных предоперационных результатов или менее опытных операторов дополнительное рекомендуется использование внутрисердечной эхокардиографии (ICE) или ЧП-Эхо. Оба метода усложняют процедуру, первая требует дополнительного венозного доступа, для чего требуется интубация или, по крайней мере, глубокая седация для оптимального комфорта и безопасности пациента.
[nextpage title=»Техника закрытия дефекта МПП»]
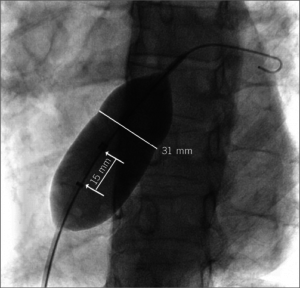
ДМПП проходимы так же, как и ООО. После введения проводника проводят оценку размера дефекта с помощью раздутия баллона (balloon sizing) с учетом только жесткого ободка. Следует избегать случайного увеличения дефекта при расширении баллона, и есть несколько способов обеспечить атравматическую калибровку. Баллон накачивается разбавленным контрастом либо непосредственно находясь в пределах дефекта, либо еще в левом предсердии и только затем втягивается в дефект. Баллон раздувается до тех пор, пока с обоих сторон не будет визуализироваться четкая «талия» (рисунок 8). Если используется УЗИ, баллон раздувается до тех пор, пока доплеровский шунт через дефект не прекратится (калибровка методом flow-stop).
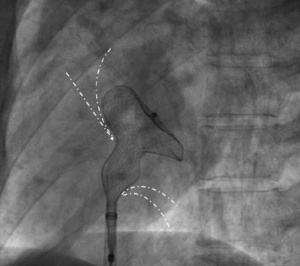
Размер устройства ASO (диаметр талии) должен быть в диапазоне 120% -150% от диаметра растянутого баллоном дефекта. Более крупный размер необходим в случае сложной стабилизации раздутого баллона, который указывает на непрочный подвижный ободок. Как и в случае с закрытием ООО, после подготовки устройства система доставки продвигается в левое предсердие. Устройство вводится в систему доставки и развивается до тех пор, пока левый предсердный диск, соединитель и небольшая часть правого предсердного диска не будут развернуты в левом предсердии, что будет подтверждено флюороскопически в проекции LAO (рисунок 9).
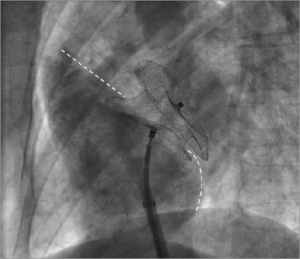
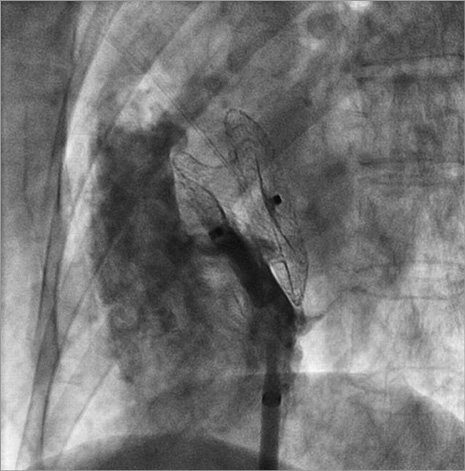
Развертывание небольшой части правого предсердного диска гарантирует, что устройство вытягивается через центр дефекта, тем самым предотвращая пролапс левого верхнего диска до того, как правый диск будет раскрыт окончательно. Вся система оттягивается назад, пока левый предсердный диск не опирается на левую предсердную сторону предсердной перегородки. Затем кончик системы доставки удаляется еще дальше, после чего правая предсердная часть устройства полностью разворачивается в правом предсердии. Для обеспечения размещения устройства в устойчивом положении выполняется мягкое шевеление. Потенциальный воздух продувается из оболочки, а для уточнения контуров правого предсердия и положения межпредсердной перегородки выполняется контрастная ангиограмма (рисунок 10). После введения контраста можно оценить положение левой границы межпредсердной перегородки. Если используется эхокардиография, проверяется положение перегородки между дисками. Если устройство позиционировано правильно, система доставки откручивается вращением против часовой стрелки и устройство освобождается. Для финальной оценки расположения устройства можно выполнить повторное контрастирование (особенно если не использовалось ультразвуковая визуализация). На этом этапе можно выявить наличие остаточных шунтов или исключить другие потенциальные проблемы (рисунок 11).
После процедуры закрытия система доставки удаляется, а гемостаз достигается ручным сжатием места венозной пункции. Это может быть выполнено самим пациентом, поскольку в бедренной вене лежащего пациента нет заметного давления.
[nextpage title=»Сопутствующая медикаментозная терапия»]
Интраоперационно пациенту вводятся антикоагулянты с нефракционированным гепарином (например, 5000 единиц или до ACT> 250 с). Одна доза антибиотика вводится в операционной или непосредственно перед процедурой, а затем в течение следующих 12 часов добавляются еще одна-две дозы, хотя использование антибиотиков не подтверждается доказательствами.
Ацетилсалициловая кислота 100 мг один раз в день в течение пяти месяцев и клопидогрель 75 мг один раз в день в течение одного-трех месяцев назначаются для антитромботической защиты, опять-таки целиком эмпирически.
Перед выпиской следует выполнить трансторакальное Эхо , чтобы подтвердить правильное положение устройства. Рекомендуется повторить Эхо через 6 месяцев после операции (лучше ЧП-Эхо), чтобы исключить остаточные шунты, проблемы с устройством или появление тромбов.
Маленькие остаточные шунты допустимы, поскольку они не имеют гемодинамического значения, и устройство отфильтровывает частицы. В случае значительного остаточного шунта рекомендуется имплантация второго устройства, что приводит к полному закрытию дефекта примерно в 90% таких случаев.
[nextpage title=»Нюансы и возможные осложнения»]
Из-за высокой эффективности и низкой частоты осложнений при использовании современных устройств, подходящие ДМПП предпочтительно закрывать интервенционно, а не хирургически. В 2005 году более 50% всех обработанных ДМПП были закрыты интервенционно, и к настоящему времени на фоне значительного развития катетерных техник процент пациентов, получающих интервенционное лечение, неуклонно растет.
Принятие решения не всегда бывает однозначным. Во-первых, это касается закрытия малых ДМПП, особенно в детском возрасте без расширения правого предсердия и правого желудочка и соотношением Qp: Qs <1,5: 1.Все плюсы и минусы профилактического закрытия мелких и гемодинамически незначительных шунтов у педиатрических пациентов остаются спорными. Во-вторых, в случае множественных дефектов или больших дефектов с малыми или отсутствующими ободками решение вопроса о необходимости закрытия может быть сложным. Наличие нескольких дефектов не является противопоказанием для закрытия устройства, но стратегия должна быть соответствующим образом скорректирована. Устройство, специально разработанное для пациентов с множественными дефектами перегородки, представляет собой окклюдер Amplatzer Cribriform, который характеризуется дисками одинакового размера и маленькой шейкой.
Если несколько дефектов расположены на значительном расстояние друг от друга, для закрытия всех шунтов может потребоваться несколько устройств, что приведет к значительному увеличению количества имплантатов и возможному риску остаточных шунтов, тромбоза и т. д. Кроме того, обод вокруг дефекта, который является ключевой структурой для фиксации устройства, может быть небольшим или частично отсутствовать, что часто имеет место в ASD Secundum. Эта ситуация не обязательно будет препятствовать закрытию устройства и может быть преодолена конкретными методами и маневрами (например, начальное освобождение устройства в правой верхней легочной вене, использование специально предварительно сформированных систем доставки и т. д.). Тем не менее, пациент должен быть проинформирован о более высоком риске возможных осложнений и остаточного шунтирования. В обоих случаях необходимо взвесить возможность хирургического закрытия.
Осложнения закрытия ДМПП/ООО зависят от опыта оператора, типа используемого устройства и характеристик дефекта (таблица 3). Риск эмболизации практически не существует при закрытии ООО в опытных руках. При закрытии ДМПП существует небольшой риск эмболизации, особенно в случаях с большими дефектами, дефектными или гибкими ободками или при несоответствии дефекта и устройства. Поскольку это обычно происходит сразу после развертывания, в зависимости от места эмболизации, устройство часто может быть извлечено без необходимости операции (например, эмболизация легочной артерии). Эмболизация аорты может потребовать хирургического вмешательства. Воздушная эмболия является одним из наиболее распространенных осложнений, приводящих к преходящей ишемии миокарда или временным неврологическим событиям, но обычно без постоянных клинических осложнений.
Другими связанными с процедурой осложнениями являются предсердные аритмии, которые наблюдаются довольно часто, но обычно протекают недолго. Если пациент остается в фибрилляции предсердий – назначается стандартная терапия. Атриовентрикулярный блок после закрытия дефекта, требующий имплантации кардиостимулятора или эксплантации устройства, был описан, но чрезвычайно редок, поскольку проводящие пути в предсердиях многочисленны. Инфекции, эрозия клапанов или блокирование кровотока из легочных вен или коронарного синуса — это другие потенциальные проблемы, которые редко встречаются.
| Осложнение | Время возникновения после операции |
| Дислокация / Эмболизация устройства | Острый или краткосрочный период |
| Тампонада | Острый или краткосрочный период |
| Повреждение митрального клапана | Острый или краткосрочный период |
| Тромбоэмболия / Инсульт | Острый, краткосрочный или среднесрочный период |
| Осложнения в месте пункции | Острый период |
| Неполное закрытие дефекта МПП | В любом периоде |
| Предсердные эрозии | Средне- и долгосрочный период |
| Эрозии аорты | Средне- и долгосрочный период |
| Предсердные аритмии | В любом периоде |
Тем не менее, в опытных центрах с большими объемами операций интервенционно закрывается до 100% дефектов, а уровень осложнений крайне низок. Поэтому у большинства пациентов с подходящими дефектами терапией выбора является интервенционное закрытие. Оптимальный подбор пациентов, дальнейшее совершенствование устройств и методов и прогнозирование возможных проблем позволяют достичь хорошего результата у пациентов, перенесших интервенционное закрытие дефектов предсердной перегородки.
Перевод статьи Tools & Techniques: Patent foramen ovale and atrial septal defect closure из журнала Eurointervention . Авторы оригинального текста и изображений — Mladen Pavlovic, MD; Lutz Büllesfeld, MD; Bernhard Meier, MD.